Linfocitos: ¡lo que debe saber!
definición
Los linfocitos son un subgrupo altamente especializado de leucocitos, los glóbulos blancos que pertenecen al sistema inmunológico, el propio sistema de defensa del cuerpo. Su nombre se deriva del sistema linfático, ya que aquí es donde son particularmente comunes.
Su tarea principal es principalmente defender el cuerpo contra patógenos como virus o bacterias. Para ello, determinadas células se especializan en un solo patógeno, por lo que se habla del sistema inmunológico específico o adaptativo.
Pero también ayudan a eliminar las células corporales mutadas, las llamadas células tumorales, que pueden provocar cáncer. Se hace una distinción entre los linfocitos B y T, así como las células asesinas naturales, cada una con funciones diferentes.

Función de los linfocitos
Si un patógeno ingresa al cuerpo, primero es absorbido y descompuesto por células de defensa inespecíficas como los macrófagos ("células gigantes que comen"). Los macrófagos a su vez muestran fragmentos del patógeno, los denominados antígenos, en su superficie y así activan las células T auxiliares, que actúan como mediadoras entre las diferentes células inmunes específicas, los linfocitos. Los linfocitos aseguran que el sistema inmunológico sea muy adaptable y pueda reaccionar de una manera finamente regulada a diferentes amenazas.
La siguiente reacción se divide en respuesta inmunitaria humoral y celular:
La respuesta inmune humoral (= los fluidos corporales) se basa en los anticuerpos, una cierta forma de proteínas, que son producidas y liberadas por las células plasmáticas. Está diseñado principalmente para patógenos que pueden multiplicarse por sí mismos, por ejemplo, bacterias, pero también otros organismos unicelulares. Los anticuerpos pueden, por ejemplo, adherirse a la superficie de las bacterias y agruparlas debido a su forma especial (aglutinación). Esto, a su vez, facilita que las células inmunes inespecíficas encuentren el patógeno y lo eliminen. Los anticuerpos también pueden cumplir otras funciones (ver Linfocitos B).
La respuesta inmune celular se centra principalmente en los virus, pero también en ciertas bacterias, que no pueden vivir por sí mismas y, por lo tanto, tienen que atacar las células del cuerpo. Si una célula es atacada, puede mostrar fragmentos del parásito en receptores especiales en su superficie. Las células T asesinas destruyen las células infectadas y así evitan la propagación del patógeno.
Leer más sobre este tema: sistema inmune como Linfocitos T
Anatomía y desarrollo de los linfocitos.
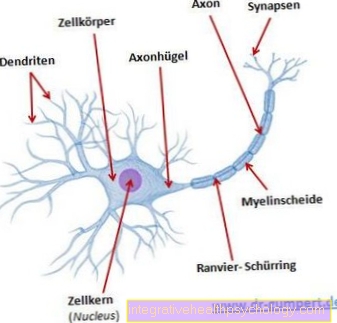
Los linfocitos tienen un tamaño muy variable, de 6 a 12 µm, y son particularmente notables debido al núcleo grande y oscuro que llena casi toda la célula. El resto de la célula puede verse como un borde citoplásmico delgado en el que solo hay unas pocas mitocondrias para la producción de energía y ribosomas para la producción de proteínas.
Se supone que las formas más grandes de los linfocitos, que también tienen un núcleo celular más ligero (= eucromático), fueron activadas por un ataque bacteriano o viral. Los linfocitos inactivos más pequeños, que también se denominan ingenuos, son mucho más comunes en personas sanas y tienen aproximadamente el mismo tamaño que los glóbulos rojos (eritrocitos).
Leer más sobre: Eritrocitos
Los linfocitos surgen a través de la etapa intermedia de los linfoblastos a partir de las células madre hematopoyéticas (hematopoyesis = formación de sangre), la mayoría de las cuales se encuentran en la médula ósea en los adultos. Aquí, las células precursoras (progenitoras) de los linfocitos se diferencian de las de las otras células (mieloides) en que algunas de ellas continúan madurando en el timo (también llamadas mollejas). Posteriormente se denominan linfocitos T ("T" de timo). La maduración en el timo persigue el propósito de clasificar todas aquellas células T que reaccionan a las propias estructuras del cuerpo o que tienen restringida su función (selección positiva y negativa).
Para más información, ver: Linfocitos T
Los linfocitos B y las células NK (células asesinas naturales), por otro lado, completan su maduración como las otras células sanguíneas en la médula ósea ("B" para "médula ósea" o históricamente Bursa fabricii, un órgano de las aves). Una vez que los linfocitos B han abandonado la médula ósea como células maduras, vírgenes (= no especializadas), entran en órganos como el bazo, las amígdalas o los ganglios linfáticos, donde pueden entrar en contacto con antígenos (estructuras extrañas). Para ello, la célula lleva ciertos anticuerpos en su superficie, que sirven como receptores de células B. Las llamadas células dendríticas, otro tipo de célula inmunitaria que no pertenece a los linfocitos, presentan fragmentos de antígeno a los linfocitos B vírgenes y los activan con la ayuda de las células T auxiliares. Si se ha activado una célula B, se divide varias veces y se transforma en una célula plasmática (selección clonal).
Los diferentes tipos de linfocitos tienen un aspecto muy similar, pero se pueden diferenciar unos de otros utilizando métodos especiales de marcado y tinción (inmunohistoquímica) bajo el microscopio.
Linfocitos B
Cuando se activa, la mayoría de las células B maduras se convierten en células plasmáticas, cuya tarea es formar anticuerpos contra sustancias extrañas. Los anticuerpos son proteínas en forma de Y que pueden unirse a estructuras muy específicas, los llamados antígenos. En su mayoría son proteínas, pero a menudo también azúcares (carbohidratos) o lípidos (moléculas grasas). Los anticuerpos también se denominan inmunoglobulinas y se dividen en 5 clases según su estructura y función (IgG, IgM, IgD, IgA e IgE).
Los anticuerpos ahora ayudan de diversas formas a combatir la infección: por ejemplo, se pueden neutralizar venenos como la toxina del tétanos o se puede marcar todo el patógeno. Un patógeno marcado de esta manera ahora puede ser absorbido y digerido por ciertas células inmunes, los macrófagos y los neutrófilos. Sin embargo, el patógeno también puede ser destruido y disuelto por células asesinas naturales, así como macrófagos y granulocitos por sustancias que son venenosas para el patógeno. Algunos anticuerpos también pueden aglutinar las células diana para hacerlas más fáciles de detectar y hacerlas más receptivas.
Otra forma es a través de la activación del sistema del complemento, que está formado por varias proteínas inespecíficas que disuelven las células marcadas en una especie de reacción en cadena. Sin embargo, estas proteínas están presentes permanentemente en concentraciones comparables en la sangre y son parte del sistema inmunológico innato. Además, los mastocitos son activados por anticuerpos, que liberan sustancias inflamatorias como la histamina, que aumentan el flujo sanguíneo al tejido afectado y así facilitan que otras células inmunes lleguen al foco de inflamación.
Usted también puede estar interesado en: histamina
Otro subgrupo de linfocitos B se convierte en células de memoria B cuando se activa, que pueden sobrevivir durante varios años. Si el cuerpo se vuelve a exponer al mismo patógeno durante este tiempo, estas células pueden convertirse en células plasmáticas mucho más rápidamente para evitar que la infección se propague de manera más eficiente. Esto crea una protección de vacunación que dura mucho tiempo y puede durar años.
Para obtener información detallada, consulte también: ¿Qué son los linfocitos B?
Linfocitos T
Hay dos grupos principales de linfocitos T, células T auxiliares y células T asesinas, así como células T reguladoras y, a su vez, células T de memoria de larga duración.
Las células T auxiliares fortalecen el efecto de las otras células inmunes al unirse a los antígenos que se presentan en otras células inmunes y luego liberan citocinas, una especie de atrayente y activador de otras células inmunes. Dependiendo del tipo de células de defensa requeridas, existen otros subgrupos especializados. Desempeñan un papel especial en la activación de las células plasmáticas y las células T asesinas.
Las células T asesinas también se denominan linfocitos T citotóxicos porque, a diferencia de la mayoría de las células inmunitarias, destruyen sus propias células en lugar de las que son ajenas al cuerpo. Esto siempre es necesario cuando una célula del cuerpo es atacada por un virus u otro parásito celular o cuando una célula se modifica de tal manera que podría convertirse en una célula cancerosa. La célula T killer puede adherirse a ciertos fragmentos de antígeno que la célula infectada lleva en su superficie y matarlos a través de varios mecanismos. Un ejemplo particularmente conocido es la introducción de una proteína de los poros, perforina, en la membrana celular. Esto hace que el agua fluya hacia la celda objetivo, provocando que estalle. También puede inducir la autodestrucción de la célula infectada de manera controlada.
Las células T reguladoras tienen una función inhibidora sobre las otras células inmunes y, por lo tanto, aseguran que la reacción inmunológica no continúe acumulándose y pueda desaparecer rápidamente nuevamente. También juegan un papel importante en el embarazo, ya que garantizan que las células del feto, que en última instancia también son extrañas, no sean atacadas.
Al igual que las células de memoria B, las células de memoria T se conservan durante mucho tiempo y también garantizan una respuesta inmune más rápida si el patógeno reaparece.
Células asesinas naturales
Las células asesinas naturales o células NK desempeñan un papel similar al de las células asesinas T, pero a diferencia de los otros linfocitos, no pertenecen al sistema inmunológico adaptativo sino al innato. Eso significa que son permanentemente funcionales sin tener que activarse de antemano. Sin embargo, es difícil regular su respuesta. Sin embargo, pertenecen a los linfocitos, ya que surgen de las mismas células progenitoras.
Leer más sobre el tema.
- sistema inmune
- ¿Cómo se puede fortalecer el sistema inmunológico?
Valores normales de los linfocitos
La concentración de linfocitos fluctúa a lo largo del día y depende de la hora del día, el estrés, el esfuerzo físico y otros factores. Se habla de un aumento patológico solo si los linfocitos están por encima de los valores límite.
Para determinar la cantidad de linfocitos, necesita un recuento sanguíneo diferencial, que es parte del recuento sanguíneo grande. La proporción de linfocitos en el recuento total de leucocitos (leucocitos = glóbulos blancos) debe estar entre el 25 y el 40%, lo que corresponde a una concentración de 1.500-5.000 / µl. Si el valor está por encima de este, se habla de linfocitosis, si está por debajo de él se llama linfocitopenia (también llamada linfopenia). En los niños pequeños, la concentración de leucocitos puede ser significativamente mayor y la proporción de linfocitos puede llegar a 50 %.
Leer más sobre: Conteo de glóbulos
¿Cuál puede ser la causa si aumentan los linfocitos?
Infecciones como causa de un aumento de linfocitos.
En la mayoría de los casos, un mayor número de linfocitos (= linfocitosis) indica una infección viral, ya que los linfocitos son particularmente adecuados para combatirlos. Básicamente, con todas las infecciones por virus, es de esperar al menos una concentración de linfocitos ligeramente mayor.
Además, determinadas infecciones bacterianas como la tos ferina (tos ferina, tos con palo), tuberculosis (tisis), sífilis, tifus (fiebre entérica, fiebre de los padres) o brucelosis (fiebre mediterránea, fiebre de Malta) desencadenan un aumento característico de linfocitos. El número de linfocitos permanece aumentado incluso con cursos crónicos, es decir, de larga duración. Otros parásitos como Toxoplasma gondii también pueden conducir a un aumento a corto plazo de linfocitos.
Leer más sobre: Enfermedades infecciosas
Enfermedades autoinmunes
Sin embargo, también existen enfermedades inflamatorias sin infección que conducen a un aumento del número de linfocitos, como B. las enfermedades intestinales Morbus Crohn y colitis ulcerosa, así como enfermedades autoinmunes como Morbus Graves, en las que los linfocitos forman anticuerpos contra las células tiroideas, por lo que estas se excitan demasiado, lo que a su vez perturba el equilibrio hormonal. La sarcoidosis (enfermedad de Boeck), un tipo especial de inflamación que afecta con especial frecuencia a los pulmones, también puede provocar un aumento en la cantidad de linfocitos.
Puede encontrar más información aquí: Sarcoide
Enfermedad de tiroides
Sin embargo, un equilibrio alterado de las hormonas tiroideas, como en el caso de una tiroides hiperactiva (hipertiroidismo) o la enfermedad de Addison (insuficiencia suprarrenal primaria), también puede conducir a un aumento del número de linfocitos.
Usted también puede estar interesado en: la enfermedad de Addison
Aumento de leucocitos debido a enfermedades tumorales.
Se puede desarrollar linfocitosis particularmente grave en ciertas neoplasias malignas, es decir, células tumorales malignas:
En la leucemia linfocítica crónica (LLA), son las células precursoras de los linfocitos las que se han convertido en células cancerosas debido a mutaciones. Es la forma más común de leucemia en el mundo occidental. Dado que ocurre con especial frecuencia alrededor de los 50 años, también se la conoce como "leucemia de la edad".
La leucemia linfoblástica aguda también surge de las células precursoras de linfocitos, pero suele ir acompañada de una rápida degeneración de la médula ósea, que puede provocar anemia, ya que las otras células sanguíneas no pueden desarrollarse adecuadamente. Como resultado, en algunos casos no se puede determinar ningún cambio o incluso una disminución en los leucocitos totales. El número anormalmente aumentado de linfocitos solo se puede ver en el recuento sanguíneo diferencial.
Dado que los linfocitos mutados generalmente no funcionan en ambas enfermedades, se puede suponer un rendimiento reducido del sistema inmunológico a pesar del aumento del número.
Además, otros tumores malignos (malignos) que afectan a otras células del sistema linfático pueden desencadenar linfocitosis, por ejemplo, el linfoma de Hodgkin (enfermedad de Hodgkin, linfogranulomatosis, linfogranuloma), pero también ciertos linfomas no Hodgkin.
Lea también: linfoma de Hodgkin como leucemia
¿Cuál puede ser la causa si los linfocitos están bajos?
La linfocitopenia a menudo ocurre como resultado de la terapia y no se considera patológica en este contexto: esto es particularmente común cuando se trata con corticoides, especialmente cortisona, y cuando se administra globulina antilinfocítica. Ambos se utilizan específicamente para suprimir reacciones inflamatorias. Otras formas de terapia que pueden causar deficiencia de linfocitos son la radiación y la quimioterapia, las cuales se usan para la terapia del cáncer, pero también pueden afectar las células del cuerpo que se dividen rápidamente, como las precursoras de las células sanguíneas. Además, este fenómeno se observó cuando se administró el fármaco ganciclovir, que se utiliza principalmente para tratar el citomegalovirus (CMV, herpesvirus humano 5, HH5). Durante el tratamiento con luz ultravioleta de onda larga (UVA), la sustancia natural psoraleno a menudo se coadministra debido a su efecto fotosensibilizante, que también puede tener un efecto reductor sobre el recuento de leucocitos.
Otra posible razón de la linfocitopenia es la desnutrición de bajo contenido proteico o el estrés persistente, que pueden aumentar permanentemente el nivel de cortisol (ver terapia con cortisona). Además, también existen cuadros clínicos de causa orgánica como la enfermedad de Cushing, que estimula la médula suprarrenal para producir un aumento de cortisol debido a un mal funcionamiento de la glándula pituitaria (adenohipófisis). Ciertas enfermedades autoinmunes como la artritis reumatoide, el lupus eritematoso sistémico (liquen mariposa) y la enteropatía exudativa (gastro) (síndrome de Gordon) también pueden provocar linfopenia.
En la uremia, debido a un mal funcionamiento del riñón, se acumulan sustancias en la sangre que, en personas sanas, se eliminan a través de la orina. Además de una serie de otros síntomas, esto también conduce a una disminución de la función de los leucocitos.
Dado que una infección por el virus HI (virus de la inmunodeficiencia humana, desencadena el SIDA) afecta y destruye particularmente las células T colaboradoras, es de esperar también aquí una fuerte caída en el número de linfocitos.
También existen causas congénitas que afectan principalmente al desarrollo de los linfocitos (linfocitopoyesis) y se desencadenan por mutaciones en los genes de ciertas enzimas. Estos incluyen la deficiencia de adenosina desaminasa y la deficiencia de nucleósido fosforilasa de purina, así como el síndrome de Wiskott-Aldrich, que afecta principalmente a los trombocitos (plaquetas sanguíneas) debido a la formación deficiente del citoesqueleto, la linfocitopenia y la inmunodeficiencia generalmente solo se desarrollan en años posteriores. de vida.
Además, ciertos linfomas de Hodgkin (enfermedad de Hodgkin, linfogranulomatosis, linfogranuloma) y linfomas no Hodgkin individuales, es decir, cáncer de todo el sistema linfático, pueden afectar el desarrollo de los linfocitos y, en consecuencia, reducir su número.
Lea también: Miastenia gravis o VIH
¿Cómo cambian los linfocitos con un resfriado?
Los términos cotidianos resfriado y infección similar a la gripe significan una serie de diferentes enfermedades leves del tracto respiratorio, que en su mayoría son causadas por virus, pero ocasionalmente también por bacterias.
Es típico de las infecciones bacterianas que el número total de leucocitos aumente (= leucocitosis), lo que generalmente también afecta a los linfocitos. En las infecciones virales, la cantidad total de leucocitos tiende a ser menor (= leucopenia), lo que a menudo se debe al hecho de que el sistema inmunológico no puede seguir el ritmo de la producción de células de defensa, pero ciertos virus también pueden inhibir el sistema inmunológico directamente. Sin embargo, es característico que el número de linfocitos permanezca estable o incluso aumente, ya que estos son particularmente adecuados para combatir infecciones virales y, por lo tanto, se desarrollan preferentemente a partir de las células madre comunes.
¿Cómo cambian los linfocitos en el VIH?
El virus HI (virus de la inmunodeficiencia humana) ataca las células que tienen una proteína de superficie específica, la CD4 (grupo de diferenciación). Se trata principalmente de células T auxiliares, que son destruidas por la replicación del virus, lo que reduce drásticamente el número de linfocitos (linfopenia). La pérdida de células T auxiliares funcionales supera la cantidad de células infectadas, por lo que también deben influir los mecanismos de inhibición indirecta, que afectan, por ejemplo, a la maduración de los linfocitos. Los macrófagos (células gigantes de fobia) también son atacados, aunque estos no cuentan entre los linfocitos y solo una proporción comparativamente pequeña muere.
En la primera fase, alrededor de 1 a 4 semanas después de la infección (infección primaria), los pacientes a menudo muestran síntomas similares a los resfriados durante aproximadamente una semana. Sin embargo, la cantidad de leucocitos generalmente aumenta ligeramente aquí, mientras que la cantidad de linfocitos disminuye. Esto suele ir seguido de un período sin síntomas en el que la cantidad de linfocitos solo disminuye muy lentamente, permanece estable o incluso se normaliza. Esta afección puede durar varios años y, a menudo, pasa desapercibida hasta que, si no se trata, eventualmente se convierte en SIDA.
Se puede encontrar más información sobre el VIH. aquí.
Vida útil de los linfocitos
La vida útil de los linfocitos puede ser muy diferente debido a las diferentes tareas: los linfocitos que nunca entran en contacto con antígenos (estructuras de cuerpo extraño) mueren después de unos días, mientras que los linfocitos activados, por ejemplo, las células plasmáticas, pueden sobrevivir durante aproximadamente 4 semanas. Las células de memoria son las que sobreviven más tiempo, ya que pueden sobrevivir durante varios años y contribuir así a la memoria inmunológica.
Según hallazgos más recientes, también hay células plasmáticas de larga vida que aún producen anticuerpos apropiados incluso después de que la infección ha disminuido y, por lo tanto, aseguran un título de anticuerpos estable (= nivel de dilución).
Por lo general, la inmunidad de por vida solo se logra con vacunas vivas, por lo que es de esperar que una porción extremadamente pequeña e inofensiva de la vacuna permanezca en el organismo.
¿Qué es la prueba de transformación de linfocitos?
La prueba de transformación de linfocitos (LTT) es un método para la detección de linfocitos T especiales, cada uno de los cuales se ha especializado en un determinado antígeno (fragmento de cuerpo extraño). Recientemente se ha utilizado principalmente en el diagnóstico de la función inmunológica, pero también en alergología para la detección de alergias a ciertos medicamentos o metales, que se manifiestan solo después de un retraso. Actualmente se recomienda principalmente como complemento de la prueba del parche. Esta prueba es una prueba de provocación para detectar alergias de contacto. Además, el valor informativo como prueba de detección de ciertos patógenos como la enfermedad de Lyme se está discutiendo actualmente de manera controvertida.
En el primer paso de la prueba de transformación de linfocitos, los linfocitos se separan de las demás células sanguíneas mediante varios procesos de lavado y centrifugación (un proceso que descompone los componentes sanguíneos según su masa). A continuación, las células, junto con el antígeno de prueba, se dejan solos durante unos días en condiciones óptimas de crecimiento. Una muestra de control permanece sin antígeno.16 horas antes de la evaluación, se agrega timina marcada radiactivamente, un componente del ADN. Una vez transcurrido el tiempo, se mide la radiactividad del cultivo de linfocitos y se calcula a partir de esto un denominado índice de estimulación. Esto proporciona información sobre si los linfocitos T son sensibles al antígeno y cuán sensibles son.
La prueba aprovecha el hecho de que las células T activadas, que surgen cada vez más de las células T de memoria sensibilizadas, se convierten o se transforman en respuesta al antígeno correspondiente. Como resultado, también comparten, por lo que tienen que construir ADN y, por lo tanto, incorporar cada vez más la timina radiactiva.
Tipificación de linfocitos
La tipificación de linfocitos, también conocida como estado inmunológico o inmunofenotipificación, es un proceso que examina la formación de varias proteínas de superficie, generalmente los llamados marcadores CD (Cluster of Differentiation). Dado que estas proteínas difieren en los diferentes tipos de linfocitos, se puede crear un patrón de expresión de las proteínas de superficie mediante el uso de anticuerpos codificados por colores producidos artificialmente. A partir de esto, se pueden sacar conclusiones sobre la distribución de los diferentes tipos, pero también sobre el grado de diferenciación de las células. Por tanto, este método es particularmente adecuado para la clasificación de leucemias, pero también se utiliza, por ejemplo, para controlar las infecciones por VIH.
Usted también puede estar interesado en: Leucemia o infección por VIH.
Linfocitos en la orina
El aumento del número de linfocitos en la orina se denomina linfocituria, que ocurre con especial frecuencia en infecciones virales, linfomas y reacciones de rechazo después de un trasplante de riñón sin un aumento de las otras células inmunitarias.
En la mayoría de los casos, sin embargo, solo se considera el número de todos los leucocitos en el contexto del estado de la orina, por lo que uno solo pensaría en una causa patológica a partir de una concentración de más de 10 / µl. Dicha leucocituria se produce a menudo en relación con una infección del tracto urinario, pero también puede tener otras causas, como inflamación de la próstata, una enfermedad reumática o un embarazo. Se habla entonces de leucocituria estéril, ya que no se pudieron encontrar bacterias además del aumento del número de leucocitos.
Linfocitos en el LCR
El líquido cefalorraquídeo, es decir, el líquido en el que nada nuestro cerebro, es comparativamente pobre en células, de las cuales, sin embargo, los linfocitos T constituyen la mayoría. Aquí es normal una concentración de 3 / µl. Además, también hay monocitos aislados, los precursores de los macrófagos ("fobia a los gigantes"). La presencia de otras células sanguíneas ya se considera patológica.
Si la barrera sangre-licor, que controla qué sustancias pueden pasar de la sangre al licor, permanece intacta, solo estos dos tipos de células aumentan en consecuencia. Este es el caso, por ejemplo, de la meningitis (meningitis), borreliosis o sífilis, pero también de enfermedades libres de infección como la esclerosis múltiple o tumores cerebrales especiales, así como de determinadas lesiones cerebrales.